L'
acido carbonico è un
acido debole, la cui formula è H
2CO
3. Il
carbonio è ibridizzato sp
2. Il suo relativo
anione è lo
ione carbonato.
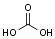
Struttura chimica dell'acido carbonico.
Biosintesi
L'acido carbonico può essere sintetizzato in due vie. Una prima via, non catalizzata, prevede la reazione spontanea di acqua con il diossido di carbonio, un ossido conosciuto come anidride carbonica. La reazione è, tuttavia, lenta. Un secondo meccanismo, favorito da un enzima, avviene grazie all'anidrasi carbonica, la quale catalizza la reazione appena riportata aumentandone la velocità.
Dissociazione dell'acido carbonico
L'acido carbonico è un acido diprotico, poiché - in soluzione acquosa - perde due atomi di idrogeno. In acqua l'acido carbonico si dissocia nello ione bicarbonato che, per la presenza di una carica negativa, è classificato come anione. Lo ione bicarbonato, successivamente, si dissocia in ione carbonato. Questa dissociazione ha un importante ruolo biologico.
Biologia dell'acido carbonico
La formazione di acido carbonico è strettamente correlata al ciclo biogeochimico dell'anidride carbonica. La maggior parte dell'acido carbonico, biologicamente attivo, è prodotto nei mari a seguito della reazione dell'anidride carbonica con l'acqua. A differenza dell'ossigeno molecolare, l'anidride carbonica reagisce - in una reazione all'equilibrio chimico - portando alla formazione di acido carbonico che, nelle successive dissociazioni porta alla formazione prima di uno ione bicarbonato (HCO-3) e successivamente di ione bicarbonato (CO--3).
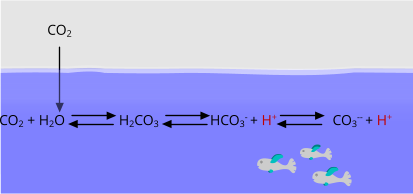
Schematizzazione del processo di acidificazione degli oceani, a opera dell'acido carbonico.
Feedback
Il tuo aiuto è importante. Ti chiediamo un minuto per rispondere a questo breve sondaggio
Come valuteresti questo articolo?
Vuoi suggerirci qualcosa?