Gli oligopeptidi ciclici rappresentano particolari peptidi, formati da 20-40 aminoacidi le cui estremità C-terminali e N-terminali possono essere libere oppure condensate tra loro a formare una molecola ciclica. Il termine deriva dal greco ed è formato da "oligo" che vuol dire "poco" e "peptide" che fa riferimento ai peptidi.
Gli oligopeptidi ciclici, dal punto di vista della frequenza di distribuzione, non sono molto frequenti poiché, nella maggior parte dei casi, i peptidi - specialmente con le estremità libere - non possiedono condensazioni e conseguenti ciclizzazioni all'interno della struttura molecolare.
Esempi di oligopeptidi biologicamente attivi
La vasopressina e l'ossitocina sono due ormoni peptidici che presentano una condensazione attraverso gli atomi di zolfo di due cisteine. Ambedue gli aminoacidi possiedono estremità n-terminali e c-terminali libere.
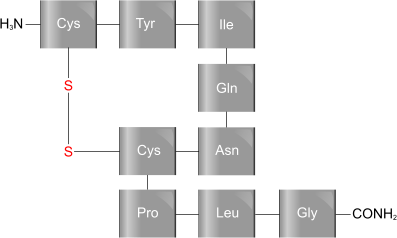
Struttura semplificata dell'
ossitocina un tipico esempio di oligopeptide ciclico.
Introduzione ai carboidrati: Introduzione e classificazione dei carboidrati, Struttura e chiralità degli zuccheri, monosaccaridi, disaccaridi, polisaccaridi. Glucosio e mutarotazione del glucosio.
Introduzione ai lipidi: I lipidi
Introduzione agli aminoacidi: Aminoacidi, carica ionica degli aminoacidi, punto isoelettrico, legame peptidico.
Metabolismo degli aminoacidi: Transaminazione, ciclo dell'urea.
Metabolismo dei carboidrati: Glicolisi, , regolazione della glicolisi, regolazione del metabolismo del glucosio, gluconeogenesi, via dei pentoso fosfati, glicogenolisi. Regolazione del glucosio ematico.
Ciclo di Krebs: Decarbossilazione ossidativa del piruvato.
Introduzione alle proteine: Proteine e struttura (struttura primaria, struttura secondaria, struttura terziaria alfa-elica, foglietto beta), enzimi, emoglobina.
Feedback
Il tuo aiuto è importante. Ti chiediamo un minuto per rispondere a questo breve sondaggio
Come valuteresti questo articolo?
Vuoi suggerirci qualcosa?