Il termine “zucchero” identifica una molecola che contiene esclusivamente idrati del carbonio, in altre parole una molecola formata esclusivamente da carbonio, idrogeno ed ossigeno. Nei capitoli successivi, sarà oggetto di discussione la capacità di “coniugarsi” di queste molecole con altri gruppi funzionali, ad esempio fosforici, per formare zuccheri con dei gruppi aggiunti o sostituiti.
Lo zucchero più semplice è la D-gliceraldeide:
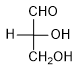
Struttura della D-gliceraldeide
La D-gliceraldeide possiede un particolare gruppo ossidrile (-OH) ed un gruppo aldeidico (-CHO). La D-gliceraldeide è una molecola chirale in quanto il carbonio centrale è ibridizzato sp3 e presenta quattro sostituenti differenti che sono -CHO, -H, -OH e -CH2OH.
Gli zuccheri non sono esclusivamente caratteristici della funzionalità aldeidica giacché possono avere una funzionalità chetonica. Per questo motivo si possono distinguere zuccheri aldeidici e zuccheri chetonici.
Il diidrossiacetone è lo zucchero chetoso più semplice:
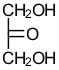
Struttura del diidrossiacetone.
Il diidrossiacetone presenta un carbonio carbonilico in “mezzo” alla molecola che è ibridizzato sp2 e forma tre legami (carbonio trivalente) di cui uno doppio legante l'ossigeno.
Chiralità degli zuccheri
Durante il primo decennio del '900 si scoprì che i composti che possiedono un carbonio sostituito con quattro classi differenti, come la gliceraldeide, nonostante abbiano proprietà chimico-fisiche equivalenti, ad esempio possiedono un simile punto di ebollizione, riescono a ruotare la luce polarizzata in modo differente. In altre parole quella che sarà chiamata D-gliceraldeide (la cui D vuol dire destrogiro) ruota la luce polarizzata di +180° mentre la L-gliceraldeide (L come levogiro) la ruota di -180°.
La caratteristica della gliceraldeide, nelle due sue forme, di riuscire a ruotare la luce polarizzata non è casuale ma è indice di una configurazione sterica particolare, riferibile alla posizione tridimensionale dell'ossidrile legato al carbonio numero 2.
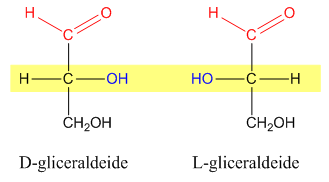
Confronto tra L-Gliceraldeide e D-Gliceraldeide
Esistono due stereoisomeri della gliceraldeide: D-gliceraldeide ed L-gliceraldeide. La molecola che per convenzione grafica è disegnata con l'ossidrile a destra prende il nome di D-gliceraldeide mentre la L-gliceraldeide, sempre per convenzione grafica, possiede l'ossidrile a sinistra. Deve essere chiaro il fatto che disegnando una molecola, sia con le proiezioni di Fischer sia con le proiezioni di Haworth, non è definita esattamente la sua struttura tridimensionale ma è semplificata la struttura e la configurazione “reale” della stessa. Il carbonio ibridizzato sp3, ad esempio, non forma angoli di 90° come si potrebbe evincere dalla formula di struttura di Fischer ma angoli di circa 109°. Inoltre i sostituenti non giacciono tutti sullo stesso piano, come erroneamente si potrebbe pensare, bensì sono disposti lungo le tre dimensioni.
Il diidrossiacetone non possiede centri chirali perché non soddisfa le condizioni necessarie di chiralità, avendo i carboni ibridizzati sp3 sostituiti con due elementi uguali, ovvero gli idrogeni, e un carbonio carbonilico di tipo chetonico.
Quella che, in realtà, può apparire una banale differenza di conformazione è di fondamentale importanza per la vita animale, compresa quella umana, ed anche per la comprensione di alcuni meccanismi biochimici. Sarà analizzato più avanti che la conformazione chirale degli zuccheri rende possibile una assoluta specificità per un enzima che, in altre parole, avrà la propria azione di catalizzatore su un enantiomero anziché su un altro.
Introduzione ai carboidrati: Introduzione e classificazione dei carboidrati, Struttura e chiralità degli zuccheri, monosaccaridi, disaccaridi, polisaccaridi. Glucosio e mutarotazione del glucosio.
Introduzione ai lipidi: I lipidi
Introduzione agli aminoacidi: Aminoacidi, carica ionica degli aminoacidi, punto isoelettrico, legame peptidico.
Metabolismo degli aminoacidi: Transaminazione, ciclo dell'urea.
Metabolismo dei carboidrati: Glicolisi, , regolazione della glicolisi, regolazione del metabolismo del glucosio, gluconeogenesi, via dei pentoso fosfati, glicogenolisi. Regolazione del glucosio ematico.
Ciclo di Krebs: Decarbossilazione ossidativa del piruvato.
Introduzione alle proteine: Proteine e struttura (struttura primaria, struttura secondaria, struttura terziaria alfa-elica, foglietto beta), enzimi, emoglobina.
Feedback
Il tuo aiuto è importante. Ti chiediamo un minuto per rispondere a questo breve sondaggio
Come valuteresti questo articolo?
Vuoi suggerirci qualcosa?