Gli aminoacidi o amminoacidi rappresentano una vasta classe di molecole biologiche e organiche, presenti sia in forma libera sia "aggregati" in complessi più o meno complessi chiamati peptidi o, in base alla lunghezza della catena, in proteine.
Gli aminoacidi, legati tra loro attraverso il legame peptidico, rappresentano i cosiddetti mattoni strutturali dei complessi proteici.
Esistono molti tipi di aminoacidi, che differiscono sul piano delle proprietà chimiche, per la capacità di formare differenti tipi di strutture peptidiche/proteiche, specialmente per quanto riguarda la disposizione spaziale. In linea generale, ogni organismo possiede un differente tipo di pool di aminoacidi sia per conformazione chimica, sia per classe di appartenenza.
Struttura degli aminoacidi
Gli aminoacidi sono formati da un gruppo aminico e da gruppo carbossilico legati a un carbonio, al quale è ulteriormente legato un idrogeno e un residuo che caratterizza l'aminoacido.
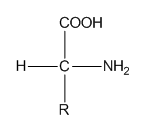
Struttura generica di un aminoacido
Chiralità degli aminoacidi
Gli aminoacidi, a eccezione della glicina, possiedono un carbonio con ibridizzato sp3. Il carbonio, inoltre, è legato a quattro sostituenti differenti e, per questa ragione, è un carbonio chirale. La presenza di un centro chirale, negli aminoacidi e in qualsiasi altra molecola, rende possibile l'esistenza di due molecole definite enantiomeri. Gli enantiomeri degli aminoacidi sono classificati in D-aminoacidi e L-aminoacidi, in base alla loro "sovrapponibilità" con l'enantiomero di riferimento che è la gliceraldeide.
Serie L e serie D degli aminoacidi
| Serie L |
Serie D |
|---|
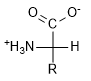
L-Aminoacido |
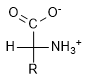
D-Aminoacido |

D-Aminoacido |

D-Gliceraldeide |
È importante sottolineare che la serie L- e la serie D- degli aminoacidi sono rappresentate con i gruppi aminici, rispettivamente, a sinistra e a destra soltanto per una convenzione grafica, in altre parole la molecola - nel suo spazio tridimensionale - non possiede un gruppo aminico "a destra" o "a sinistra" ma, semplicemente, una differente disposizione nello spazio.
Nel regno vegetale, le cellule possiedono sia aminoacidi appartenenti alla serie L- sia alla serie D-. Nel mondo animale, uomo compreso, gli aminoacidi appartengono esclusivamente alla serie L-. Per questa ragione, quando il riferimento a una cellula animale è certo, si tende a omettere la serie utilizzando, ad esempio, il nome semplice dell'aminoacido senza anteporre la serie.
Aminoacidi alpha, beta, gamma
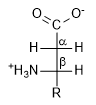
Un altro tipo di classificazione si basa sulla presenza del gruppo aminico a livello della catena carboniosa; in questo caso gli aminoacidi si classificano in base alla distanza del gruppo aminico rispetto al carbonio più ossidato, che è quello del gruppo carbossilico. La presenza del gruppo aminico nel carbonio direttamente legato al carbossile classifica la molecola come alpha-aminoacido; se tra il carbonio che lega il gruppo aminico e il carbonio carbossilico vi è un terzo carbonio (-CH2-) la molecola fa parte dei beta-aminoacidi.
Alpha e beta aminoacidi
| Alpha |
Beta |
|---|
Alpha aminoacidiBeta aminoacidi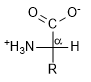 |
 |
In natura, la maggior parte degli aminoacidi, appartiene alla classe degli alpha-aminoacidi. Tuttavia, anche negli esseri superiori, alcune particolari molecole possiedono beta-aminoacidi caratteristici.
Biochimica degli aminoacidi
Dal punto di vista chimico e biochimico, gli aminoacidi presentano molte caratteristiche peculiari. Gli aminoacidi possiedono un gruppo aminico e un gruppo carbossilico, oltre a eventuali altri gruppi nel residuo. Per questa ragione la loro struttura presenta due o più gruppi ionizzabili. Il carbossile, può trovarsi in forma ionizzata (-COO-) oppure in forma protonata (-COOH) e, allo stesso tempo, anche il gruppo aminico può essere protonato (-NH3+) o deprotonato (-NH2). La ionizzazione deriva direttamente dal pH della soluzione nella quale l'aminoacido si trova e, per questo motivo, deriva anche dal valore di pK del gruppo.
In linea generale, in un sistema biologico, il gruppo carbossilico si trova nello stato ionizzato (-COO-) mentre il gruppo aminico è protonato (-NH3+).
In base al pK del carbossile, del gruppo aminico e di eventuali altri gruppi ionizzabili, ogni aminoacido possiede uno specifico punto isoelettrico.
Aminoacidi non proteinogenici
Non tutti gli aminoacidi sono inclusi nelle proteine e prendono il nome di aminoacidi non proteinogenici. Alcuni aminoacidi, ad esempio, non hanno ruolo strutturale né nelle proteine complesse né nei semplici peptidi. Nella vasta classe deii metaboliti secondari, ad esempio, è noto che alcune molecole derivano da aminoacidi non proteinogenici che subiscono delle reazioni enzimatiche per la biosintesi del metabolita secondario.
Nutrizione e aminoacidi
Gli aminoacidi rappresentano una componente fondamentale nel quadro nutrizionistico. Vengono assunti principalmente mediante l'alimentazione; è credenza comune che gli aminoacidi siano presenti soltanto nella carne e nei derivati. Tuttavia molti aminoacidi sono presenti anche nella frutta, nei legumi e nella verdura.
Aminoacidi essenziali
L'uomo è capace di sintetizzare, in altre parole di creare da sé, una piccola parte di tutti gli aminoacidi normalmente presenti nel pool cellulare. La restante parte prende il nome di aminoacidi essenziali poiché devono essere necessariamente assunti con la dieta. Gli aminoacidi essenziali sono i seguenti:
Introduzione ai carboidrati: Introduzione e classificazione dei carboidrati, Struttura e chiralità degli zuccheri, monosaccaridi, disaccaridi, polisaccaridi. Glucosio e mutarotazione del glucosio.
Introduzione ai lipidi: I lipidi
Introduzione agli aminoacidi: Aminoacidi, carica ionica degli aminoacidi, punto isoelettrico, legame peptidico.
Metabolismo degli aminoacidi: Transaminazione, ciclo dell'urea.
Metabolismo dei carboidrati: Glicolisi, , regolazione della glicolisi, regolazione del metabolismo del glucosio, gluconeogenesi, via dei pentoso fosfati, glicogenolisi. Regolazione del glucosio ematico.
Ciclo di Krebs: Decarbossilazione ossidativa del piruvato.
Introduzione alle proteine: Proteine e struttura (struttura primaria, struttura secondaria, struttura terziaria alfa-elica, foglietto beta), enzimi, emoglobina.
Feedback
Il tuo aiuto è importante. Ti chiediamo un minuto per rispondere a questo breve sondaggio
Come valuteresti questo articolo?
Vuoi suggerirci qualcosa?