In chimica, si definisce con l'ordine di legame la quantità di legami covalenti presenti tra due atomi, da intendersi come la metà della differenza tra gli elettroni di legame, e gli elettroni di antilegame. In altre parole, l'ordine di legame tiene conto del numero di doppietti di elettroni condivisi e aumenta all'aumentare del numero di legami.
Un legame covalente singolo si definisce con ordine di legame pari a 1 (n=1), un legame covalente doppio si definisce con ordine di legame pari a 2 (n=2), un legame triplo avrà ordine pari a 3 (n=3) e così via. Molecole con ordine di legame pari a zero (n=0) non esistono poiché non possono esistere molecole senza almeno un legame di tipo covalente.
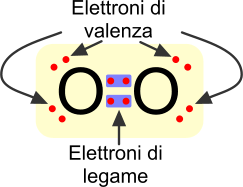
Elettroni di legame e di valenza.
Forze ed energia associata all'ordine di legame
All'aumentare dell'ordine di legame aumenta anche la forza del legame che, per questa ragione, diventa anche un indice dell'energia interna della molecola, poiché molecole più stabili possiedono, solitamente, un'energia interna inferiore rispetto a molecole meno stabili. Un legame singolo tra due atomi è meno forte rispetto a un legame doppio che, a sua volta, è meno forte se confrontato a un legame triplo.
Energia di legame e ordine di legame
| |
C-C |
C=C |
C≡ C |
|---|
| n |
1 |
2 |
3 |
| Energia (kJ / mol) |
346 |
602 |
835 |
Pagine correlate
L'atomo e la sua struttura: Nucleo (protone, neutrone) e guscio esterno (elettrone).
Proprietà dell'atomo: Numero atomico, numero di massa, peso atomico, raggio atomico.
Specie chimiche: Ossidi.
Meccanica quantistica dell'elettrone: Ipotesi di De Broglie, orbitale atomico, numero quantico principale, numero quantico secondario, spin, salto quantico.
Configurazione elettronica: ibridizzazione sp3, ibridizzazione sp2, ibridizzazione sp, struttura di Lewis.
Legame chimico: Legame debole, legame ionico, legame metallico. Regola dell'ottetto, legame covalente, legame covalente dativo, energia di legame.
Stato della materia: Solido, liquido, aeriforme (gas).
Chimica delle soluzioni: Soluzione (solvente e soluto), concentrazione (molarità , normalità , frazione molare). Idrolisi, prodotto ionico dell'acqua.
Equilibrio chimico: Legge di azione di massa, costante di equilibrio.
Feedback
Il tuo aiuto è importante. Ti chiediamo un minuto per rispondere a questo breve sondaggio
Come valuteresti questo articolo?
Vuoi suggerirci qualcosa?