Una formula chimica è un tipo di rappresentazione, testuale oppure grafica, attraverso la quale è possibile definire e fornire alcune informazioni riguardanti una molecola. In base al tipo di formula utilizzata, è possibile osservare il numero di atomi costituenti la molecola, e la loro disposizione sequenziale oltre a valutare, ove possibile, il tipo di legame chimico.
Tenendo conto del tipo di rappresentazione è possibile riportare graficamente una molecola in base alla sua formula molecolare, alla sua formula estesa oppure utilizzando al sua formula di struttura. Ciascun tipo di rappresentazione grafica fornisce dettagli differenti e, per questo motivo, si presta a differenti finalità.
Esempi di formule chimiche
| Molecola |
Formula molecolare |
Formula estesa |
Formula di struttura |
|---|
| Etanolo |
C2H6OH |
CH3CH2OH |
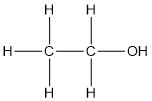 |
| Glucosio (a catena aperta) |
C6H12O6 |
C6H12O6 |
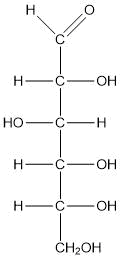 |
| Fruttosio (a catena aperta) |
C6H12O6 |
C6H12O6 |
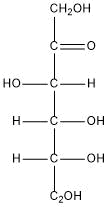 |
Formula molecolare
La formula molecolare o formula bruta fornisce informazioni sul numero di atomi che fanno parte di una molecola, senza definirne la disposizione lungo una ipotetica "catena". Per convenzione, in una formula molecolare, gli atomi sono riportati con ordine di elettronegatività crescente. Alcune classi, tuttavia, rappresentano una eccezione, ad esempio gli alcoli presentano il gruppo ossidrile (-OH) in coda e, sempre in tema di eccezione, anche l'ammoniaca (NH3) presenta l'idrogeno in coda.
Formula estesa
Nella formula estesa si riportano, graficamente, gli atomi raggruppati. In questo modo è possibile avere una sommaria idea della struttura molecolare.
Formula di struttura
La formula di struttura è un tipo di formula grafica nella quale la molecola è riportata attraverso la costruzione spaziale. Nella formula di struttura è riportato il legame chimico, sia che esso sia un legame covalente singolo, doppio o triplo e l'eventuale carica ionica.
L'atomo e la sua struttura: Nucleo (protone, neutrone) e guscio esterno (elettrone).
Proprietà dell'atomo: Numero atomico, numero di massa, peso atomico, raggio atomico.
Specie chimiche: Ossidi.
Meccanica quantistica dell'elettrone: Ipotesi di De Broglie, orbitale atomico, numero quantico principale, numero quantico secondario, spin, salto quantico.
Configurazione elettronica: ibridizzazione sp3, ibridizzazione sp2, ibridizzazione sp, struttura di Lewis.
Legame chimico: Legame debole, legame ionico, legame metallico. Regola dell'ottetto, legame covalente, legame covalente dativo, energia di legame.
Stato della materia: Solido, liquido, aeriforme (gas).
Chimica delle soluzioni: Soluzione (solvente e soluto), concentrazione (molarità , normalità , frazione molare). Idrolisi, prodotto ionico dell'acqua.
Equilibrio chimico: Legge di azione di massa, costante di equilibrio.
Feedback
Il tuo aiuto è importante. Ti chiediamo un minuto per rispondere a questo breve sondaggio
Come valuteresti questo articolo?
Vuoi suggerirci qualcosa?