Il nucleo atomico, o semplicemente nucleo, è la parte interna dell'atomo. È formato da particelle subatomiche, chiamate nucleoni che ne determinano le caratteristiche fisiche e chimiche. Le particelle subatomiche, i protoni e i neutroni sono coese tra loro, sebbene - in particolari condizioni - possano dividersi.
La presenza dei protoni classifica l'atomo all'interno del relativo elemento chimico, mentre i neutroni determinano l'eventuale isotopo. Ad esempio, il carbonio possiede sei protoni e, nella sua forma più comune (o isotopo più abbondante), possiede sei neutroni. Tutti gli atomi di carbonio, in altre parole, avranno sempre sei protoni ma, in natura, esistono anche varianti con più neutroni, chiamati isotopi del carbonio. Un isotopo stabile dell'elemento carbonio è quello con sette neutroni (7C).
Le particelle subatomiche, comprese anche gli elettroni, che non fanno parte del nucleo ma del guscio elettronico, sono qualitativamente uguali tra tutti gli elementi: è la loro quantità a determinare le caratteristiche dell'atomo.
Scoperta del nucleo
La presenza di un nucleo atomico fu considerata plausibile soltanto dopo l'esperimento di Rutherford. Attraverso il bombardamento di una lamina d'oro, si osservò che parte dei "proiettili", costituiti da particelle alpha emesse durante l'esperimento, tornavano indietro rispetto al sito bersaglio e, in parte, venivano rilevati da una lamina di solfuro di zinco (SnZn). La lamina di SnZn, nell'esperimento, aveva il ruolo di rilevatore degli urti con le particelle.
Rutherford osservò che il profilo di illuminazione della lastra era anomalo, poiché non era regolare. Ne dedusse che buona parte delle particelle alpha passasse attraverso l'atomo che, di conseguenza, non poteva avere una struttura compatta ma doveva presentava uno spazio molto marcato. Successivamente, fu avanzata un'altra ipotesi, secondo la quale una piccola parte delle particelle alpha emesse, potesse essere deviata a causa dell'impatto con questa "sconosciuta" struttura che, successivamente, fu definita nucleo atomico.
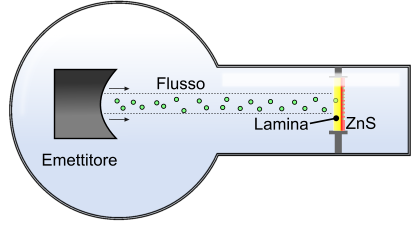
Primo esperimento di Rutherford. Un emettitore veicolava contro una lamina d'oro delle particelle alpha.
|
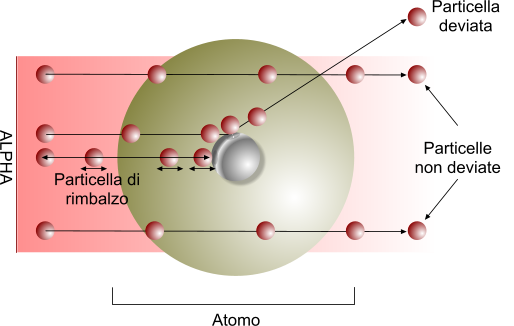
Rappresentazione schematica dell'esperimento di Rutherford.
|
Caratteristiche del nucleo
Le caratteristiche del nucleo assumono particolare importanza sia negli ambiti teorici, ad esempio per la comprensione delle proprietà e degli eventi che riguardano il nucleo, sia per la pratica sperimentale. L'avvento della meccanica quantistica ha permesso di definire dei modelli atomici teorici, ad esempio il modello atomico di Bohr, che aderiscono alle osservazioni sperimentali altrimenti incongruenti qualora si tentessa di definire, attraverso la meccanica classica, le caratteristiche e le proprietà del nucleo.
Massa nucleare
La massa nucleare rappresenta la massa del nucleo dell'atomo, ed è calcolata attraverso la somma delle masse dei costituenti alla quale si sottra l'energia di legame degli stessi protoni e neutroni.
Raggio nucleare
Il raggio del nucleo è direttamente proporzionale al numero di nucleoni in esso presenti. Per questa ragione, gli elementi con numero atomico maggiore tendono ad avere un raggio nucleare maggiore.
L'atomo e la sua struttura: Nucleo (protone, neutrone) e guscio esterno (elettrone).
Proprietà dell'atomo: Numero atomico, numero di massa, peso atomico, raggio atomico.
Specie chimiche: Ossidi.
Meccanica quantistica dell'elettrone: Ipotesi di De Broglie, orbitale atomico, numero quantico principale, numero quantico secondario, spin, salto quantico.
Configurazione elettronica: ibridizzazione sp3, ibridizzazione sp2, ibridizzazione sp, struttura di Lewis.
Legame chimico: Legame debole, legame ionico, legame metallico. Regola dell'ottetto, legame covalente, legame covalente dativo, energia di legame.
Stato della materia: Solido, liquido, aeriforme (gas).
Chimica delle soluzioni: Soluzione (solvente e soluto), concentrazione (molarità , normalità , frazione molare). Idrolisi, prodotto ionico dell'acqua.
Equilibrio chimico: Legge di azione di massa, costante di equilibrio.
Feedback
Il tuo aiuto è importante. Ti chiediamo un minuto per rispondere a questo breve sondaggio
Come valuteresti questo articolo?
Vuoi suggerirci qualcosa?