Il punto di ebollizione è un parametro, relativo alla materia presente allo stato liquido, che descrive la temperatura alla quale un liquido inizia l'ebollizione operando un passaggio dallo stato liquido allo stato solido. L'acqua, ad esempio, possiede un punto di ebollizione pari a 100°C a pressione pari alla pressione a livello del mare (760mmHg).
Ciascun liquido, o ciascuna miscela di liquidi, possiede un caratteristico punto di ebollizione che deriva sia dalle proprietà della miscela, sia dalla forza del legame debole, o forza intermolecolare, che tiene coesi gli atomi o le molecole coinvolte.
Punto di ebollizione e tensione di vapore
Da un punto di vista chimico, il punto di ebollizione coincide con l'equilibrio tra la pressione di vapore e la pressione atmosferica. L'aumento della temperatura porta a un aumento della pressione di vapore; quando la temperatura oltrepassa il punto critico di ebollizione avviene l'evaporazione, con la conseguente trasformazione della materia allo stato gassoso. Per quanto riguarda l'acqua, durante l'evaporazione si assiste alla formazione di vapore.
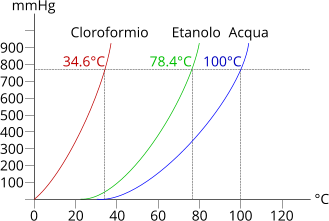
Il punto di ebollizione, varia dal tipo di liquido. L'acqua, ad esempio, inizia l'ebollizione a 100°C alla pressione di 760mmHg,
Punto di ebollizione e pressione
La pressione influisce sul punto di ebollizione poiché all'aumentare di essa aumenta anche la pressione di vapore e, di conseguenza, la temperatura necessaria affinché il liquido possa bollire e trasformarsi in vapore. Ad esempio, in una pentola a pressione, la pressione raggiunta è pari a circa 2ATM e, per questa ragione, il punto di ebollizione dell'acqua passa da 100°C a circa 120°C.
Pagine correlate
L'atomo e la sua struttura: Nucleo (protone, neutrone) e guscio esterno (elettrone).
Proprietà dell'atomo: Numero atomico, numero di massa, peso atomico, raggio atomico.
Specie chimiche: Ossidi.
Meccanica quantistica dell'elettrone: Ipotesi di De Broglie, orbitale atomico, numero quantico principale, numero quantico secondario, spin, salto quantico.
Configurazione elettronica: ibridizzazione sp3, ibridizzazione sp2, ibridizzazione sp, struttura di Lewis.
Legame chimico: Legame debole, legame ionico, legame metallico. Regola dell'ottetto, legame covalente, legame covalente dativo, energia di legame.
Stato della materia: Solido, liquido, aeriforme (gas).
Chimica delle soluzioni: Soluzione (solvente e soluto), concentrazione (molarità , normalità , frazione molare). Idrolisi, prodotto ionico dell'acqua.
Equilibrio chimico: Legge di azione di massa, costante di equilibrio.
Feedback
Il tuo aiuto è importante. Ti chiediamo un minuto per rispondere a questo breve sondaggio
Come valuteresti questo articolo?
Vuoi suggerirci qualcosa?