Lo stato della materia rappresenta l'organizzazione fisica che possiede la materia, da intendersi come sistema omogeneo oppure eterogeneo di atomi e molecole in relazione alla forma fisica anche rispetto allo spazio che la contiene. I fattori che determinano la presenza di una materia in un determinato stato sono molti e concorrenti tra loro e, allo stesso modo, anche la trasformazione da uno stato ad un altro è resa possibile dalla variazione di questi fattori.
In linea generale, una materia tende a esistere in un determinato stato qualora rimangano costanti alcune proprietà fisiche quali la temperatura e la pressione. Differenti stati di temperatura, o pressione, difatti, possono influire lo stato della materia e influenzare o impedire il passaggio verso altri stati.
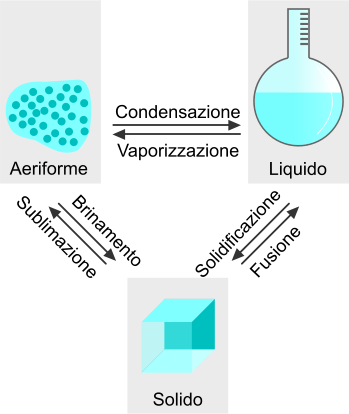
La materia si presenta, in base alle condizioni del sistema, in stati fisici diversi. Per ogni stato della materia è possibile una trasformazione verso un altro stato modificando le condizioni del sistema, quali la
pressione o la temperatura.
In chimica, è oggetto di studio sia la persistenza della materia in uno stato sia il passaggio verso un altro stato, e le relative condizioni necessarie.
Stati della materia
| Stato |
Comprimibilità |
Forma |
|---|
| Solido |
Bassa |
Il solido possiede dimensione propria |
| Liquido |
Bassa |
I liquidi prendono forma del recipiente che li contiene |
| Aeriforme |
Alta |
Tendono ad occupare il massimo spazio possibile, disponendosi in modo disordinato |
Stato solido
Nello stato solido le molecole sono aggregate tra loro, formando una struttura praticamente incomprimibile e resistente. I solidi possiedono una forma propria che non dipende da contenitori o, comunque, da un sistema di costrizione della materia.
Stato liquido
Lo stato liquido è caratterizzato da molecole legate tra loro ma che non garantiscono una forma propria alla materia. Per questa ragione, i liquidi prendono la forma dei contenitori nei quali sono immessi. I liquidi, per via della caratteristica disposizione delle molecole, sono incomprimibili.
Stato aeriforme
Lo stato aeriforme è formato da molecole non legate tra loro che tendono a disporsi occupando il massimo spazio disponibile. Gli aeriformi per questa ragione, devono essere confinati all'interno di recipienti per evitare che si disperdano nell'atmosfera. La tendenza a occupare quanto più spazio possibile, determina la bassissima resistenza alla compressione. Tra gli aeriformi si distinguono i gas, formati da molecole omogenee o eterogenee, che sono aeriformi a temperatura ambiente, e il vapore che, invece, è il prodotto della trasformazione, anche a seguito della somministrazione di calore, di un solido o un liquido.
Stato di plasma
Il plasma è uno stato della materia formato da gas altamente ionizzato, ad esempio a seguito di un processo elettrochimico che ha portato alla formazione di ioni carichi.
Passaggio di stato
Il passaggio di stato è un evento che porta la materia da uno stato, ad esempio solido, a un altro, ad esempio liquido. I passaggi di stato avvengono quando una variabile di stato, durante un intervallo di tempo, è variata. Ad esempio, alle basse temperature, la maggior parte della materia, è presente allo stato solido. In questo stato, le molecole che fanno parte della materia, possiedono una bassa energia cinetica e, in gergo chimico, "vibrano" moderatamente.
Il legame debole che tiene coese le particelle di una sostanza allo stato solido, è vinto dall'aumento della temperatura del solido stesso. Questo avviene poiché l'energia cinetica aumenta e vince la forza di attrazione che lega, debolmente, le particelle. Somministrando sufficiente energia alla materia presente allo stato solido, sotto forma di calore, tanta quanto basta per raggiungere il punto di liquefazione, le particelle diventano libere di allontanarsi, rompendo - di fatto - la loro coesione.
La trasformazione tra stato solido e stato liquido prende il nome di passaggio di stato e, per ogni tipo di trasformazione, possiede un nome specifico.
Passaggi di stato
| Stato di partenza |
Stato finale |
Nome del passaggio di stato |
|---|
| Liquido |
Solido |
Solidificazione |
| Solido |
Liquido |
Fusione |
| Liquido |
Aeriforme |
Ebollizione |
| Aeriforme |
Liquido |
Condensazione |
| Liquido |
Solido |
Solidificazione |
| Aeriforme |
Solido |
Brinamento |
Pagine correlate
L'atomo e la sua struttura: Nucleo (protone, neutrone) e guscio esterno (elettrone).
Proprietà dell'atomo: Numero atomico, numero di massa, peso atomico, raggio atomico.
Specie chimiche: Ossidi.
Meccanica quantistica dell'elettrone: Ipotesi di De Broglie, orbitale atomico, numero quantico principale, numero quantico secondario, spin, salto quantico.
Configurazione elettronica: ibridizzazione sp3, ibridizzazione sp2, ibridizzazione sp, struttura di Lewis.
Legame chimico: Legame debole, legame ionico, legame metallico. Regola dell'ottetto, legame covalente, legame covalente dativo, energia di legame.
Stato della materia: Solido, liquido, aeriforme (gas).
Chimica delle soluzioni: Soluzione (solvente e soluto), concentrazione (molarità , normalità , frazione molare). Idrolisi, prodotto ionico dell'acqua.
Equilibrio chimico: Legge di azione di massa, costante di equilibrio.
Feedback
Il tuo aiuto è importante. Ti chiediamo un minuto per rispondere a questo breve sondaggio
Come valuteresti questo articolo?
Vuoi suggerirci qualcosa?